1. 서 론
2. 실내 실험
2.1 실험 재료
2.2 시료 조성
2.3 시험 방법
3. 실험 결과 및 분석
3.1 입도 및 비중 변화
3.2 미세구조 관찰
3.3 X선 회절분석
3.4 팽창특성
3.5 전단 거동
4. 요약 및 결론
1. 서 론
팽창성 지반이란 건습에 의해 지반 재료의 팽창과 수축이 발생하는 지반을 말한다(Al-Homoud et al., 1995; Chen, 1975). 이러한 팽창성 지반 상에 구조물을 건설할 경우, 지반의 부등 변형으로 인하여 구조물에 균열이 발생하거나 기초가 융기하는 등의 큰 피해가 발생하며 복구를 위해 많은 사회적·경제적 비용이 소요된다. 팽창성 지반에 대한 기존의 연구들은 서로 다른 지역에 퇴적되어 있는 자연적 팽창성 지반(natural expansive soil)을 이용하여 팽창성 점토의 이중층수 확장에 의한 팽창량과 팽창압 변화 파악(Chen, 2012; Fredlund et al., 1995; Nelson and Miller, 1997), 팽창성 지반의 함량에 따라 전단 시 부피 팽창 거동(dilatant)에서 부피 수축 거동 (contractive)으로의 전이 거동 파악(Bayoglu, 1995) 등의 연구가 주로 이루어졌다.
팽창성 지반의 피해를 감소시키는 방법에는 크게 지반개량 공법과 기초개량 공법이 있다(Chen, 1975; Nelson et al., 2015). 지반개량 공법에는 지반의 융기를 방지하기 위한 선행침수공법과 차수공법 등이 있으며 지반의 융기량을 감소시키기 위하여 약액 주입을 통해 지반을 고결화 시키는 공법과 팽창토를 비팽창토로 치환시키는 공법 등이 있다(Chen, 1975; Nelson et al., 2015). 기초 개량공법에는 지반의 팽창에 의해 기초가 영향을 받지 않도록 슬래브를 지반과 이격시키는 공법과 지반팽창에 대한 말뚝의 저항력을 증가시키기 위해 Under-reamed pile(Sharma et al., 1978)이나 Granular pile anchor(Phanikumar et al., 2004)처럼 개량된 말뚝을 사용하는 공법 등이 있다.
근래에 들어 제강 및 제련 산업의 발달로 철강 산업이 발전함에 따라 팽창 가능성이 있는 CaO와 MgO 등이 포함된 산업 부산물이 다량 발생하고 있다. 이렇게 인공적/화학 반응에 의해 만들어진 재료가 지반에 매립되어 팽창을 야기할 경우 이러한 지반을 자연적 팽창성 지반과 구별하여 인공적 또는 화학적으로 야기된 팽창성 지반(artificially/chemically induced expansive soil)이라 부른다. 현재 국내에서는 매년 20만톤 이상의 철강부산물들이 매립되고 있는 것으로 보고되었으며(Son et al., 2002), 전 세계적으로 철강부산물이 포함된 재료로 건설된 도로가 파괴되거나 철강부산물을 매립한 지반이 융기하여 주변 건물들에 피해를 야기하는 등 인공적 또는 화학적으로 야기된 팽창성 지반에서의 피해 사례들이 보고되고 있다(Geiseler, 1996; Rohde et al., 2003; Yildirim and Prezzi, 2009). 일반적으로 팽창 가능성이 있는 산업부산물 중 MgO가, 최종 팽창량이 상대적으로 크고 반응이 완료되기까지 더 오랜 시간이 소요되기 때문에 다른 팽창성 물질들보다 더 큰 피해를 야기한다고 알려져 있다(Takano et al., 2015). 그러나 이러한 인공적 또는 화학적으로 야기된 팽창성 지반의 공학적 거동 특성 변화에 대한 연구는 아직 미미한 상태이다.
본 연구에서는 MgO 함량에 따른 혼합토의 특성을 확인하기 위하여 5가지 무게비(WMgO/WTotal=0, 30, 50, 70, 100%)를 가지는 시료를 조성하였다. 실험실 조건에서 MgO의 수화반응을 촉진시키기 위해 0.1M의 마그네슘 아세테이트(Mg(CH3COO)2, Daejung Chemical&Metal Co.)를 촉매로 사용하였고 실험 온도 조건을 70°C로 하였다(Aphane, 2007; Matabola et al., 2010). 수화반응 전·후 MgO의 광물특성을 비교하기 위해 X선 회절분석(XRD, X-Ray Diffraction)을 실시하였으며 전자 주사 현미경(FE SEM-EDS, Electron Microscope-Energy Dispersive Spectroscopy)을 통해 미세구조 변화를 관찰하였다. 또한 팽창량 시험(Free swell test)과 팽창압 시험(Swelling pressure test)을 통해 혼합토의 팽창특성을 파악하였으며 직접전단시험(Direct shear test)으로 수화반응 전·후 혼합토의 전단거동 특성을 파악하였다.
2. 실내 실험
2.1 실험 재료
본 연구에서는 인공적 또는 화학적으로 야기된 팽창성 물질로 철강부산물 중 하나인 MgO 내화벽돌(Posco Chemical Co.)을 파쇄하여 사용하였다. 혼합 전 파쇄된 MgO 내화벽돌의 입도분포를 파악하기 위하여 입도분석(ASTM-D6913 2004; ASTM-D7928 2016)을 실시하였다. 실험 시 입경에 따른 혼합토 거동에 미치는 영향을 최소화하기 위하여 Fig. 1과 같이 파쇄된 MgO의 평균입경(D50)과 유사한 평균입경을 가지는 인공파쇄사(K7 sand, Kyungin material Inc.)를 선택하여 혼합토를 조성하였다. 통일분류법(ASTM-D2488 2017)에 따르면 두 시료 모두 SP로 분류되었다. MgO의 비중(Gs)은 3.41로 인공파쇄사의 비중(2.64) 보다 상대적으로 크게 나타났다. X선 형광분석(XRF, X-ray Fluorescence, Philips PW-2404) 결과에 따르면, 수화반응 전 MgO 내화벽돌은 85.5%의 산화마그네슘(MgO)과 5.31%의 산화칼슘(CaO)으로 이루어져 있어 총 약 91%가 팽창성 물질로 구성되어있다. 본 연구에 사용된 재료의 자세한 기본 특성 및 수화반응 전 화학적 조성은 각각 Table 1 및 Table 2와 같다.
Table 1.
Index propetrties of materials used in this study
| Material | Crushed MgO | Sand |
| Specific gravity, Gs | 3.41 | 2.64 |
| Median particle size D50 [mm] | 0.22 | 0.18 |
| Coefficient of uniformity, Cu | 7.11 | 2.24 |
| Coefficient of curvature, Cc | 0.84 | 1.21 |
| USCS | SP | SP |
Table 2.
Chemical composition of materials used in this study (before hydration)
| Chemical composition [%] | ||||||||
| MgO | Al2O3 | SiO2 | CaO | Fe2O3 | K2O | P2O5 | TiO2 | |
| Crushed MgO | 85.5 | 1.41 | 4.45 | 5.31 | 2.11 | 0.25 | 0.34 | 0.05 |
| Sand | 0.07 | 0.68 | 98.41 | 0.10 | 0.50 | 0.17 | 0.01 | 0.05 |
2.2 시료 조성
5가지 무게비(WMgO/WTotal=0, 30, 50, 70, 100%)로 파쇄한 MgO를 모래와 혼합하여 시료를 조성하였다. 균질한 상태의 건조시료를 조성하기 위해 무게비에 맞추어 준비한 혼합물을 교반기를 이용하여 동일한 속도로(60rpm) 15분간 혼합하였으며 모든 시료에 동일하게 60kNm/m3의 다짐에너지를 가하였다.
2.3 시험 방법
본 연구에서는 팽창성 재료의 수화반응을 촉진시키기 위해 마그네슘 아세테이트 0.1M을 촉매로 사용하였으며 70°C의 실험온도를 유지하였다(Aphane, 2007; Matabola et al., 2010).
2.3.1 미세 구조 및 광물 조성 관찰
전자 주사 현미경(FE-SEM, Hitachi S-4800)을 이용하여 수화반응 전·후 시료의 미세 구조 변화를 관찰하였다. 또한 수화반응 전후 파쇄 MgO의 광물조성을 비교하기 위해 구리(Cu)를 음극 물질(Anode material)로 사용하여 2θ=5°~90°의 범위에서 0.02°의 분해능으로 X선 회절분석(XRD, D/Max-2500V/PC, Rigaku)을 실시하였다. 미세 구조 및 광물 조성 변화 관찰을 위한 시료는 수화반응 전의 파쇄 MgO와 수화반응 후의 Mg(OH)2를 60°C로 24시간동안 건조하여 준비하였다.
2.3.2 팽창 특성
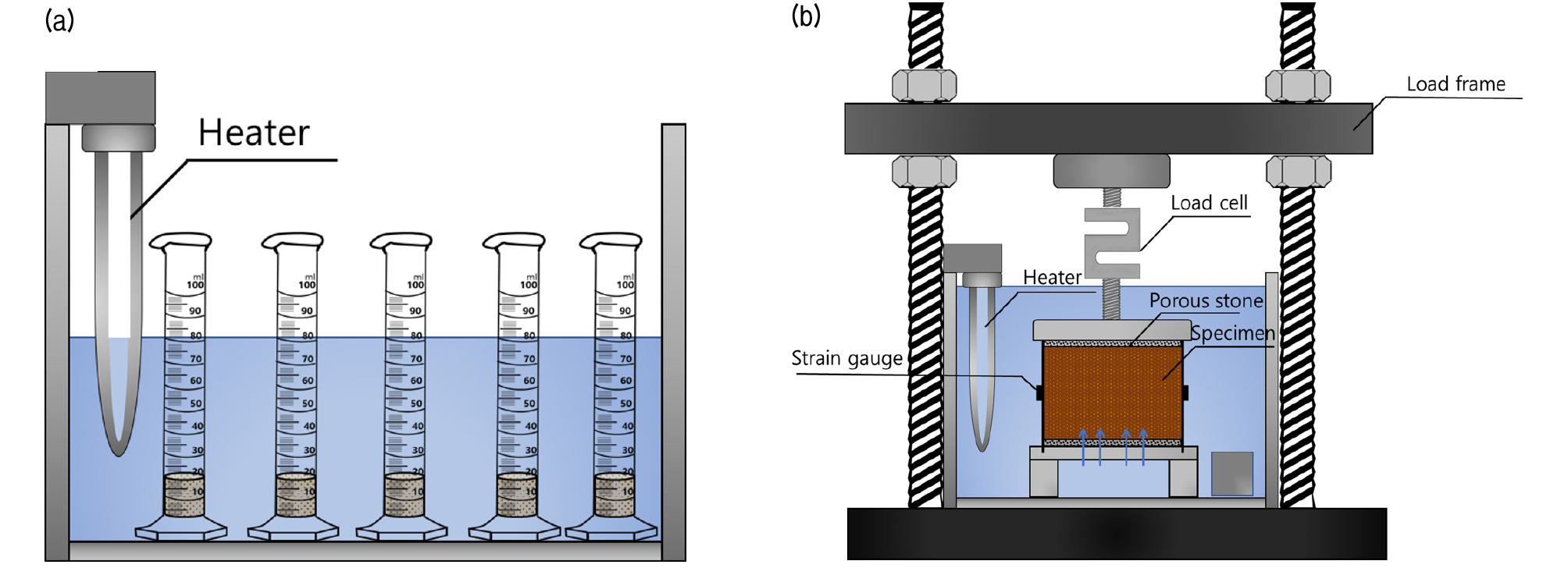
MgO의 수화반응에 따른 팽창 특성을 확인하기 위하여 자유 팽창 시험(Free swell test)과 팽창압 시험(Swelling pressure test)을 실시하였다. Fig. 2(a)와 같이 자유 팽창량 측정을 위하여 100ml 실린더에 20ml의 혼합물을 조성한 후 일정 시간 간격으로 사진을 촬영하고 이미지 분석을 통하여 시간에 따른 팽창량을 계산하였다. 팽창압 측정을 위해 50×30×1(직경×높이×두께, mm) 셀에 시료를 조성한 후 로드셀과 변형율계를 이용하여 시간에 따른 수직방향 및 수평방향 팽창압을 측정하였다(Fig. 2(b)).
2.3.3 전단거동
수화반응 과정 중에 작용하는 팽창압과 실험온도에 의한 실험 장비의 파손을 방지하기 위하여 전단실험에는 수화반응이 완료된 시료를 재성형하여 사용하였다. 그러나 수화 반응에 의해 MgO는 Mg(OH)2로 상변화를 일으키기 때문에 수화 반응 후 재료의 부피와 무게가 변화하게 된다. 자유팽창(free swell) 실험과 동일한 단위중량을 가지는 시료를 조성하기 위하여 수화반응 후 혼합물의 팽창량, 함수비 및 MgO 함량을 고려하여 재성형 시료의 단위중량(γs)은 다음 식 (1)과 같이 조성하였다.
여기서 γs는 수화반응 후 재성형 시료의 단위중량, γd는 수화반응 전 시료의 건조단위중량, 1.4는 순수한 MgO의 수화반응 후 분자량 변화를 통해 계산한 무게변화량, ω는 수화반응 후 시료의 함수비, Sw는 무게비별 혼합시료의 최종 팽창량이다. 직접 전단 실험은 100kPa, 200kPa 및 300kPa의 세가지 연직응력에서 1mm/min의 속도로 실시하였다(ASTM-D3080/D3080M 2011; ASTM-D5321 2020).
3. 실험 결과 및 분석
3.1 입도 및 비중 변화
Fig. 3은 혼합비별 수화반응 전·후 혼합토의 입도변화를 보여준다. MgO는 다음과 같은 수화반응에 의하여 Mg(OH)2로 변하게 된다(Amaral et al., 2010; Matabola et al., 2010):
1) 하이드록실화(hydroxly): MgO(solid) + H2O(liquid) → MgOH+(surface) + OH-(aqueous solution)
2) OH-이온의 MgOH+ 표면흡착: MgOH+(surface) + OH-(aq) → MgOH+·OH-(surface)
3) Mg2+ 및 OH- 이온 용해: MgOH+·OH-(surface) → Mg2+(aqueous solution)+ 2OH-(aqueous solution)
4) Mg(OH)2 석출: Mg2+(aqueous solution) + 2OH-(aqueous solution) → Mg(OH)2(solid)
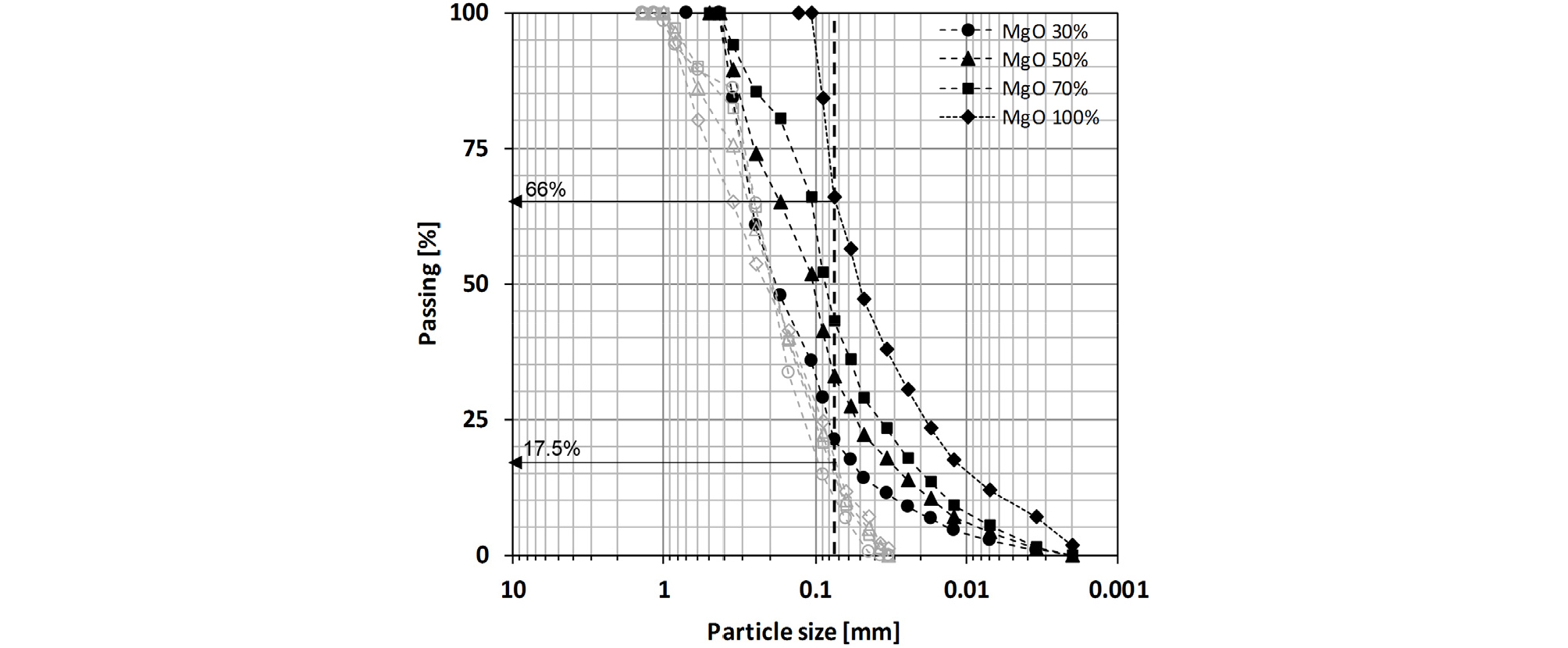
수화반응 시 MgO 표면의 분화가 일어나며 MgO는 수화반응 후 Mg(OH)2가 되며 입자크기가 감소한다. 입도분석 결과 Fig. 3과 같이 순수한 MgO의 경우 수화반응 후 #200체 통과량이 17.5%에서 66%로 증가하였다. 또한 혼합토 내 MgO 함량이 증가함에 수화 반응 후 #200체 통과율이 증가하였으며 혼합토의 평균입경 역시 감소하였다.
수화반응 결과 혼합토의 #200체 통과율이 12%를 초과함에 따라 수화반응에 따른 혼합토의 흙의 분류를 재평가하기 위하여 추가적으로 액소성한계 시험을 실시하였으며(ASTM-D4318 2017; BS1377 1990), 통일분류법에 따르면 수화반응 후 혼합토는 MgO 함량이 증가함에 따라 SM(WMgO/WTotal=30; 50%), SC(WMgO/WTotal=70%) 및 MH(WMgO/WTotal=100%)로 흙의 분류가 변하였다.
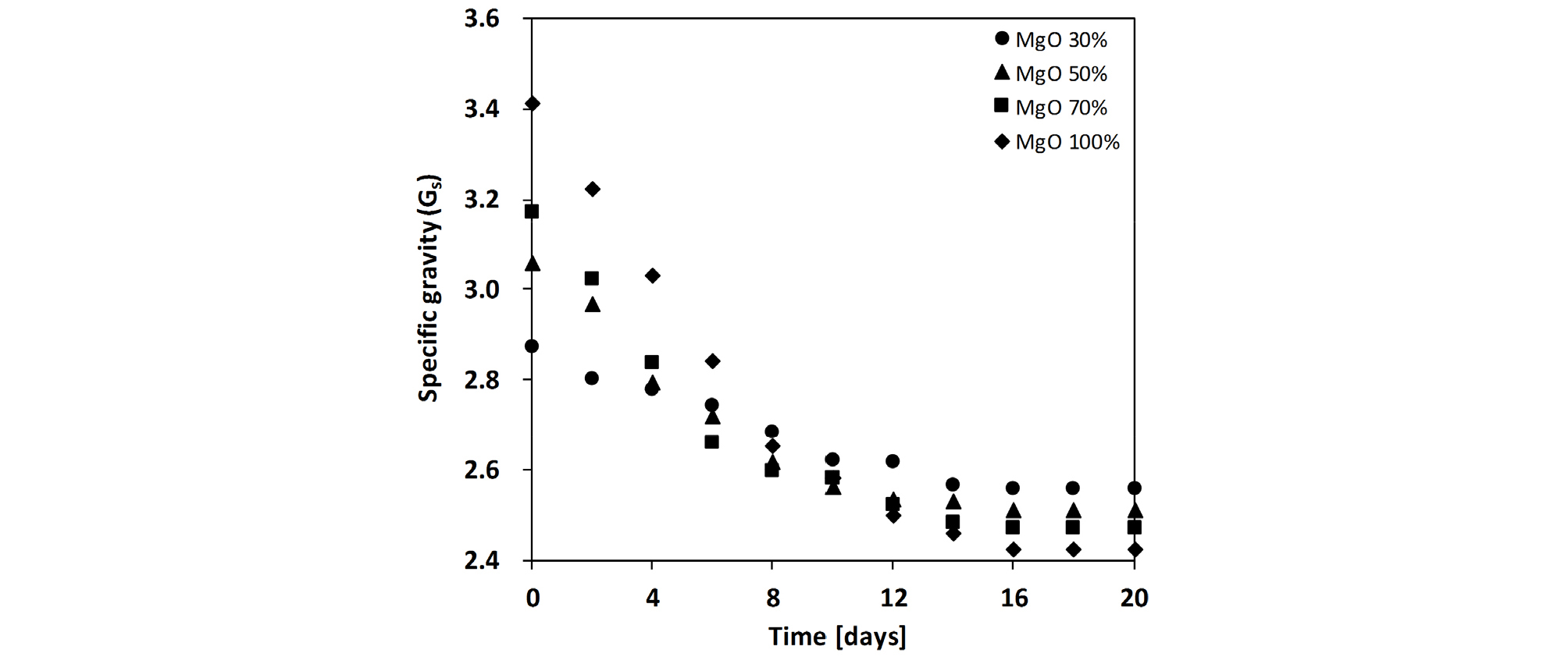
Fig. 4는 수화반응으로 인한 시간에 따른 혼합토의 비중(Gs) 변화를 보여준다. 수화반응 전 초기 혼합물은 모래에 비하여 상대적으로 큰 MgO의 비중(GsMgO) 때문에 혼합토 내 MgO 함량이 높을수록 혼합토의 비중은 높은 값을 보였다. 수화반응의 진행으로 시간에 따라 혼합토의 비중은 감소하였으며, MgO의 수화반응 결과물인 Mg(OH)2의 비중이 2.42로 수화반응이 진행될수록 혼합토의 비중은 줄어든다. 또한 Mg(OH)2의 비중이 모래의 비중(Gssand)보다 상대적으로 작기 때문에 수화반응 후 혼합토의 비중은 MgO 함량이 높을수록 상대적으로 작아져 수화반응이 진행됨에 따라 혼합토의 수화반응 전 비중값과 역전현상을 보인다.
3.2 미세구조 관찰
Fig. 5는 MgO의 수화반응 전과 수화반응 후의 미세구조 변화를 보여준다. 수화반응 전 파쇄된 MgO 입자는 둥근 입자 모양에 거친 표면을 형성하고 있다(Fig. 5(a) and (b)). 수화반응 후 육각 결정 구조(Hexagonal crystal structure)의 Mg(OH)2가 관찰되었으며 미세 입자들로 분화된 것을 확인할 수 있다(Fig. 5(c) and (d)).
3.3 X선 회절분석
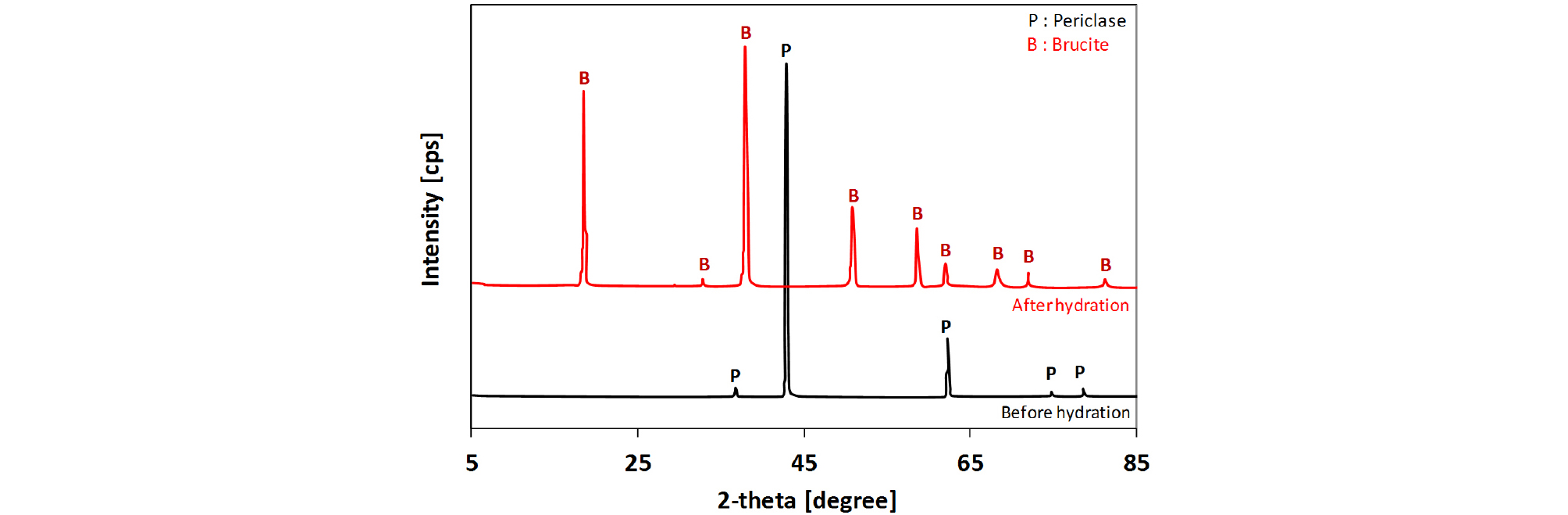
Fig. 6은 MgO의 수화반응 전 후의 XRD 패턴을 나타낸다. 수화 반응에 따라 시료의 광물학적 특성은 페리클라제(periclase)에서 수화반응 후 브루사이트(brucite)로 변화하였다.
3.4 팽창특성
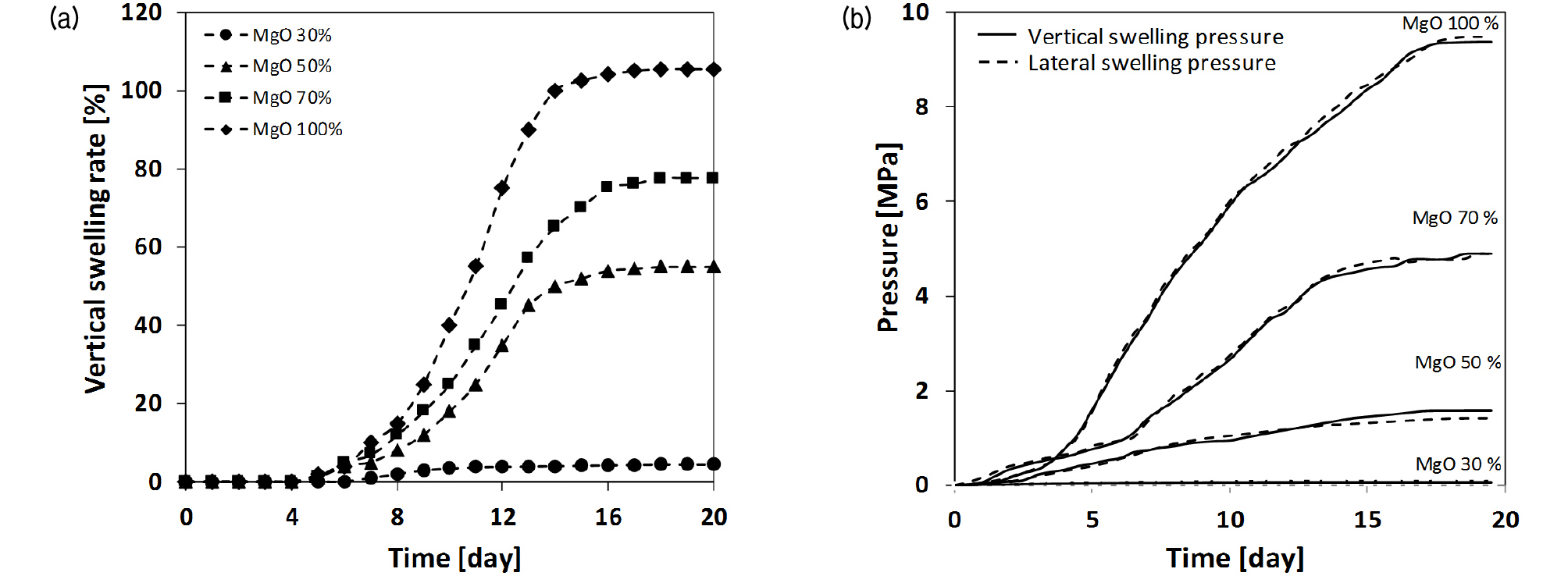
Fig. 7은 수화반응으로 인한 시간에 따른 MgO-모래 혼합토의 수직 팽창량과 수직 및 수평 팽창압 변화를 보여준다. Fig. 7(a)와 같이 혼합토 내 팽창성 물질인 MgO 함량이 많을수록 팽창량은 증가하는 경향을 보였으며 MgO 100% 시료의 경우 MgO와 Mg(OH)2의 비중 차이를 통해 계산한 팽창량과 유사하게 수화반응 후 약 104%의 부피 팽창을 보였다. 팽창압은 Fig. 7(b)와 같이 MgO 함량에 따라 증가하는 것으로 나타났으며 등방성을 보였다. MgO 함량 30% 시료의 팽창압은 77kPa로 상대적으로 낮게 측정되었으나 MgO 함량 50% 시료에서 1.6MPa로 급격하게 증가하였다.
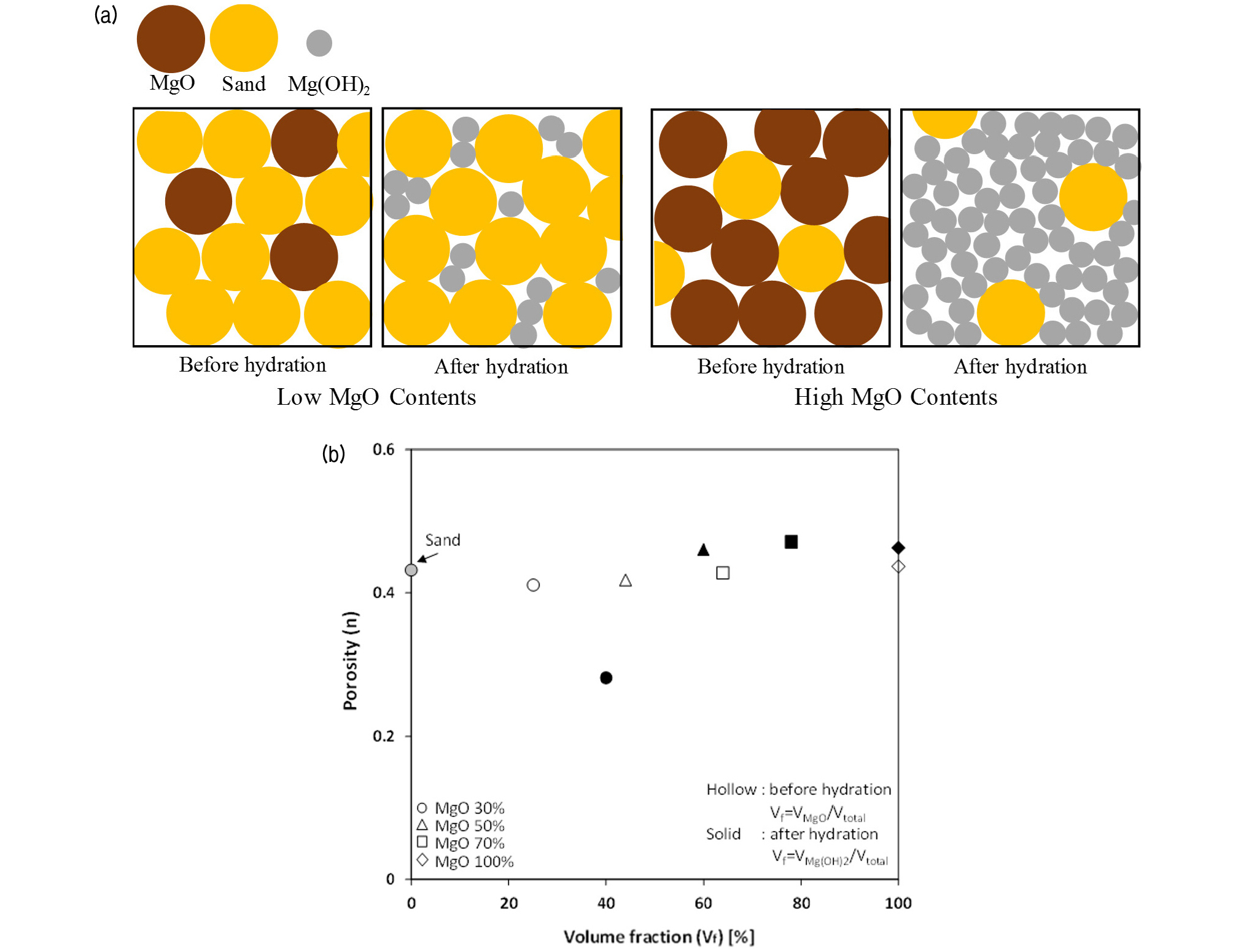
이러한 WMgO/WTotal=30% 시료의 상대적으로 낮은 팽창량과 팽창압 특성은 수화반응 전 후 시료의 공극 변화 분석을 통하여 설명된다. Fig. 8(a)는 MgO 함량에 따른 수화반응 전 후 시료의 공극 변화에 대한 모식도이다. MgO는 수화반응 후 Mg(OH)2로 화학적 변화에 따라 작은 입자들로 분화되어 세립화된다. 낮은 MgO 함량 혼합물의 경우, 수화반응에 의해 상대적으로 적은 양의 분화된 Mg(OH)2가 생성되고 생성된 Mg(OH)2 입자는 상대적으로 크기가 큰 모래 입자 사이의 공극을 주로 차지하게 된다. 그러나, 높은 MgO 함량 혼합물의 경우, 초기에는 생성된 Mg(OH)2가 모래 입자 사이의 공극을 채우지만 수화반응의 진행에 따라 Fig. 8(a)와 같이 지속적으로 생성된 Mg(OH)2가 혼합물 내의 주요 입자의 역할을 하게 된다.
수화반응 전 MgO의 부피 및 수화반응 후 Mg(OH)2의 부피와 총 시료의 부피로 계산된 부피비()에 따라 계산된 시료의 공극률의 변화는 Fig. 8(b)과 같다. 초기 무게비로 조성한 WMgO/WTotal=30%인 시료의 경우, 수화반응 후 부피비로 계산하였을 때 Mg(OH)2의 부피가 전체의 약 40% 정도를 차지하였으며 생성된 Mg(OH)2가 모래 입자 사이의 공극을 채워 수화반응 전과 비교하여 수화반응 후 공극률이 감소하였다. 이는 세립토-조립토 혼합물에서 세립토의 부피가 전체의 약 40%일 때 최소 공극을 가지는 기존의 연구 결과와 유사하다(Lade et al., 1998; Ueda et al., 2011; Vallejo, 2001). 그러나 초기 무게비 WMgO/WTotal=50%, 70%인 혼합토는 수화반응 전 MgO 및 모래로 구성된 조립질 구조에서 수화반응 후 상대적으로 세립질인 분화된 Mg(OH)2가 지배적인 세립질 구조로 바뀌게 되며 혼합토 내 세립질인 Mg(OH)2의 부피가 증가하여 조립질인 모래 입자는 서로 분리되며 Mg(OH)2가 혼합물의 간극 및 입자 배열을 지배하게 된다. 따라서 시료의 팽창을 구속한 팽창압 시험에서 MgO 함량 30% 시료는 상대적으로 낮은 팽창압을 보였으나, MgO 함량 50% 이상의 시료에서는 급격한 팽창압의 증가가 관찰되었다.
3.5 전단 거동
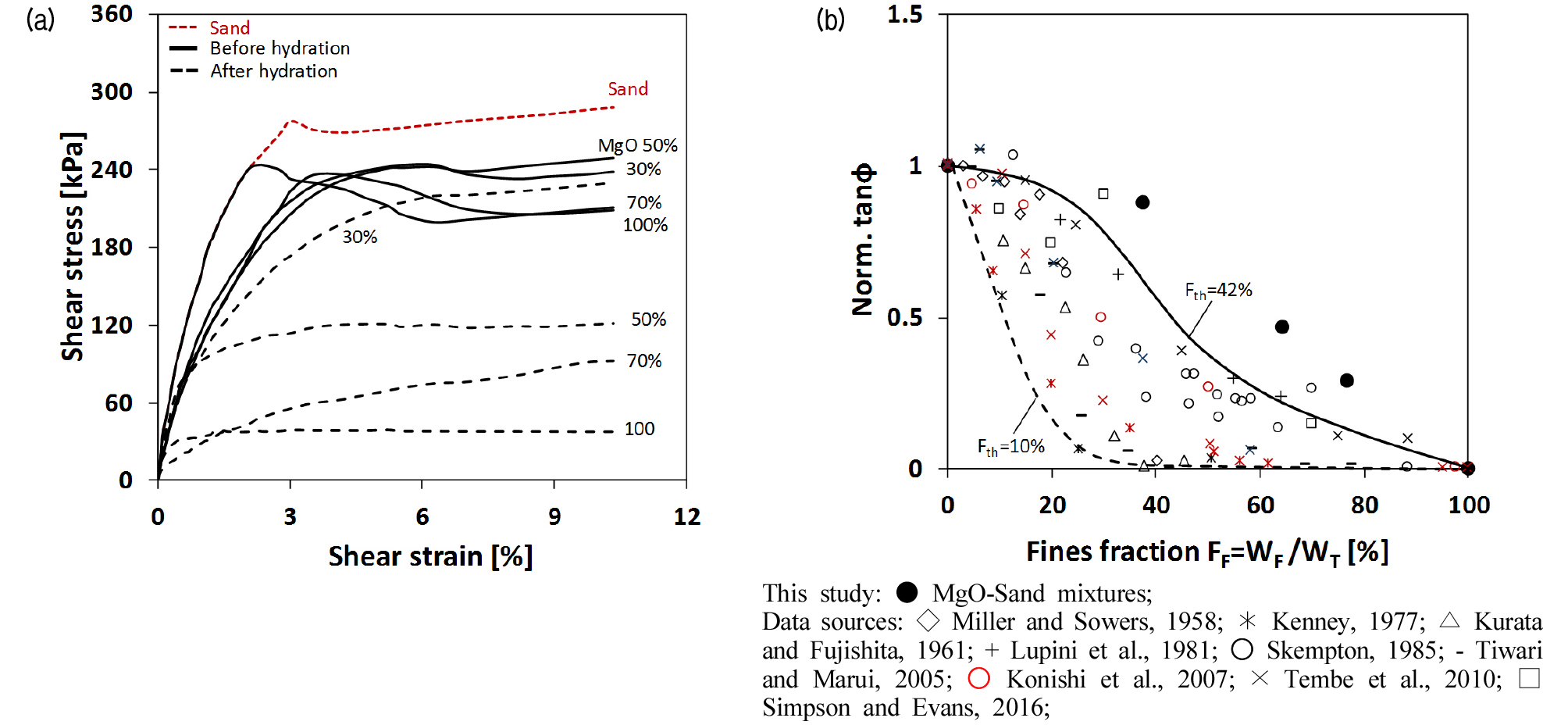
수화반응 전·후 혼합토의 전단 시 응력-변형률 곡선은 Fig. 9(a)와 같다. 수화반응 전 MgO 함량이 높을수록 MgO-모래 혼합토는 전단 시 최대전단강도(peak shear strength)가 뚜렷한 부피 팽창거동(dilative behavior)을 보였으며 낮은 MgO 함량의 혼합토는 전단 시 부피 수축거동(contractive behavior)을 보였다. 수화반응 후 혼합토의 전단강도는 MgO 함량이 높을수록 더 크게 감소하였으며, 모든 시료는 전단 시 부피 수축거동을 보였다. 수화반응 전 혼합토의 최대 마찰각은 혼합비에 따라서 34.5~38.6로 약간의 차이를 보였으나 수화반응 후 혼합토의 마찰각은 혼합비에 따라 5.8~35.8로 큰 값의 차이를 보였다.
Fig. 9(b)는 세립질 함량 (FF=WF/WT)에 따른 정규화된 의 관계를 보여준다.
여기서 C는 조립토 및 F는 세립토를 나타낸다. Fig. 9(b)에는 본 연구의 결과와 조립토-세립토 혼합물 선행 연구의(Kenney, 1977; Konishi et al., 2007; Kurata and Fujishita, 1961; Lupinl et al., 2009; Miller and Sowers, 1958; Simpson and Evans, 2016; Skempton, 1985; Tembe et al., 2010; Tiwari and Marui, 2005) 결과를 함께 도시하였다. 수화반응에 따라 MgO가 Mg(OH)2로 변화될 때, 입자 크기는 감소하지만 시료의 총 무게는 증가하기 때문에 변화한 무게를 고려하여 수화반응 후 세립질의 함량을 계산하였다. 다양한 선행 연구의 서로 다른 실험 조건에도 불구하고 모든 실험 결과에서 정규화된 전단 강도가 조립토 지배 전단 강도에서 세립토 비율이 증가함에 따라 급격히 감소하여 세립토 지배 전단 강도로의 전이 거동이 관찰된다. Park and Santamarina(2017)에 따르면 조립토-세립토 혼합물의 경우, 전이 거동의 한계 세립질 함량 (Fth)은 약 10~42% 이며 1) 두 입자의 상대 크기비가 증가하거나; 2) 액성한계가 증가하거나; 3) 조립토의 입도분포가 양호하고 둥근 입자일수록 한계 세립질 함량 (Fth)이 감소한다고 하였다. 단, 한계 세립질 함량 (Fth)은 순수 조립토와 세립토 결과의 산술평균값 (i.e., xi=(xC+xF)/2) 근처의 세립질 함량으로 정의한다(Park and Santamarina, 2017). 본 연구의 MgO-모래 혼합물의 한계 세립질 함량 (Fth)은 세립질 Mg(OH)2 비율 약 60%로 기존의 연구에 비해 다소 높은 것으로 나타났다.
4. 요약 및 결론
본 연구에서는 MgO-모래 혼합토의 팽창특성과 수화반응 전후의 전단거동을 파악하기 위하여 MgO 함량에 따라 5개의 중량비로 시료(i.e., WMgO/WTotal [%] = 0, 30, 50, 70 100)를 조성하였다. 수화반응 전·후 시료의 기본 특성시험, 혼합물의 팽창량 및 팽창압시험, 혼합물의 직접전단시험을 실시하고 그 결과를 종합해 보면 다음과 같다.
(1) MgO는 수화반응 후에 Mg(OH)2로 분화하여 입자 크기가 감소하고 소성을 띄었으며 비중은 감소하였다. 미세구조 관찰과 X선 회절분석을 통해 분석한 결과 MgO는 수화반응 전 정육면체 구조의 periclase에서 수화반응 후 육각형 구조의 brucite로 변화하였다.
(2) MgO 함량 30% 시료의 팽창량 및 팽창압은 각각 4.5% 및 77kPa로 상대적으로 작았으나 MgO 함량 50% 이상 시료에서는 팽창량은 55~104%로 상대적으로 크게 증가하였고 팽창압은 급격히 증가하는 양상을 보였다. 모래와 입경이 비슷한 MgO 입자는 수화반응 후 Mg(OH)2로 화학적 변화에 따라 분화되어 입경은 작아지고 총 부피는 증가한다. 낮은 MgO 함량의 시료에서는 수화반응 후 생성된 Mg(OH)2가 모래입자 사이의 공극을 주로 차지하게 되고, 높은 MgO 함량의 시료의 경우 생성된 Mg(OH)2가 모래 입자 사이 공극을 채운 후 모래입자 또는 다른 Mg(OH)2 입자를 밀어내기 때문으로 판단된다.
(3) 수화반응 전 높은 MgO 함량의 시료는 전단 시 부피 팽창 거동을(dilative) 보였으나 낮은 MgO 함량의 시료는 부피 수축거동을(contractive) 거동을 보였다. 수화반응 후 혼합물의 정규화된 전단강도는 Mg(OH)2의 함량이 증가함에 따라 조립질에서 세립질로 바뀌었으며, 전이 거동을 보이는 혼합토의 한계 세립질(Mg(OH)2) 함량 (Fth)은 약 60%로 기존의 연구(10~42%)에 비해 상대적 높은 것으로 나타났다.